
El anticuerpo monoclonal de nuestros test tiene una alta especificidad frente al antígeno del SARS-CoV-2 limitando la posibilidad de falsos positivos.
biotical SARS-CoV-2 Ag card test está 100% fabricado y desarrollado en España por Biotical Health S.L.U, bajo normativa Reglamento Europeo 98/79/EC para Productos Sanitarios de Diagnóstico In Vitro, así como la Certificación ISO13485.
|
¿Qué es el virus SARS-Cov-2?
El virus SARS-CoV-2 es un nuevo tipo de coronavirus responsable de la enfermedad COVID19.
COVID19 cursa con un cuadro muy amplio de síntomas entre los que destacan fiebre, fatiga, dolor de garganta, dolor de cabeza, disnea, diarrea, perdida de gusto y olfato además de complicaciones circulatorias y orgánicas de diversos tipos. SARS-CoV-2 se considera un virus respiratorio potencialmente causante de cuadros de neumonía.
El SARS-CoV-2 ha demostrado un nivel alto de transmisión entre humanos debido a su periodo de incubación prologado (de dos a doce días), la capacidad de cursar de forma asintomática en ciertos individuos y de permanecer activo en superficies.
El virus se propaga por gotas de saliva al hablar, toser o estornudar en distancias cortas y en menor medida por aerosoles.
Otras vías de transmisión como contaminación por heces son posibles.
El virus tiene su vía de entrada en la cavidad nasofaríngea donde accede a las células epiteliales y muestra su mayor carga viral en las primeros días, replicándose y accediendo a otras células del cuerpo con receptores específicos a medida que progresa la enfermedad.

biotical health
SARS-CoV-2 Ag card
Procedimiento
1º
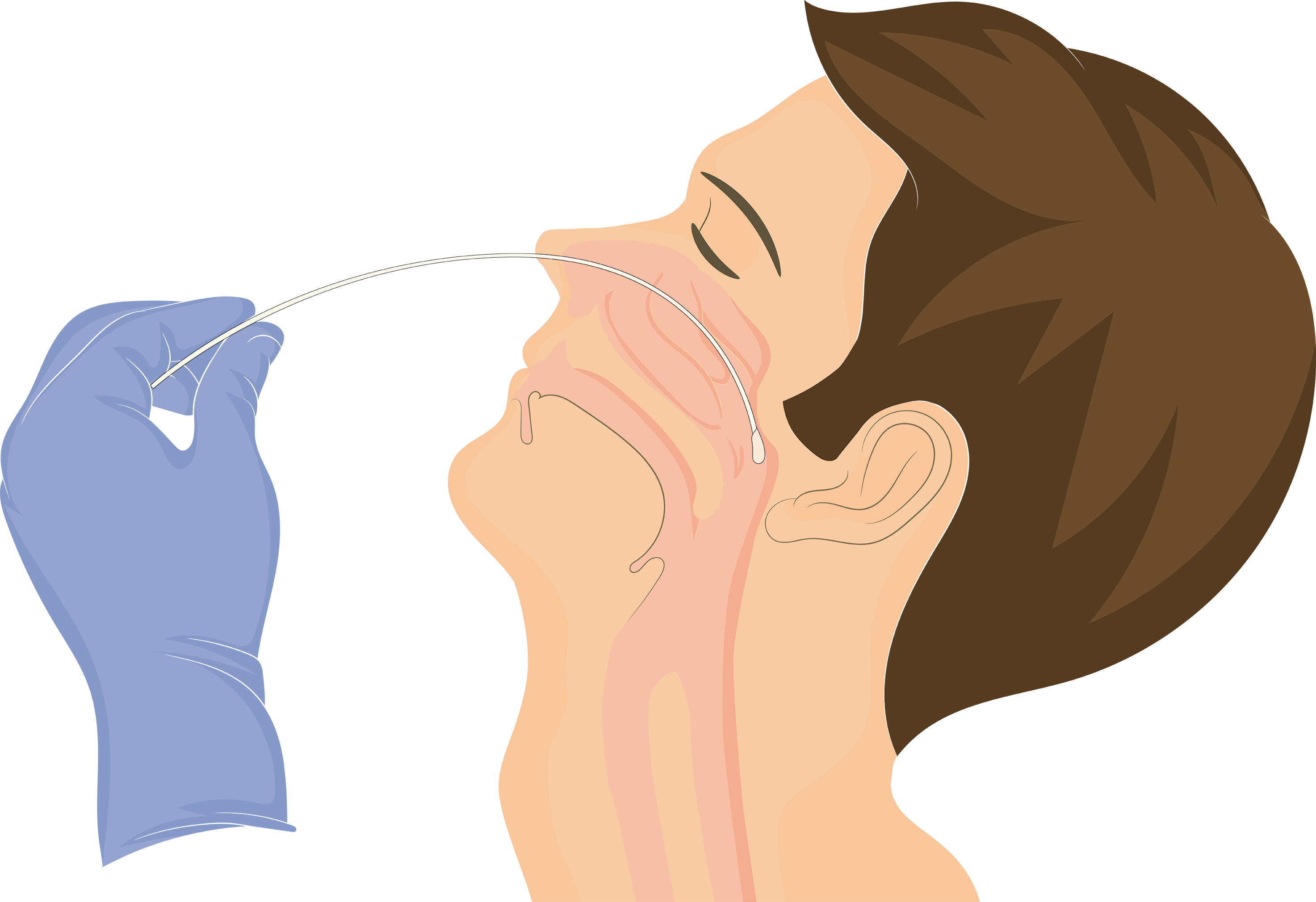
Sacar el hisopo estéril de su envase
e introducirlo hasta contactar con la nasofaringe, rotar entonces el hisopo suavemente contra la pared nasal para capturar tanto células como mocos.
2º

Introducir el hisopo en el tubo y rotarlo 1 min para extraer el líquido.
3º

4 º Leer el resultado transcurridos 10 minutos
NEGATIVO
POSITIVO
INVÁLIDO
INVÁLIDO

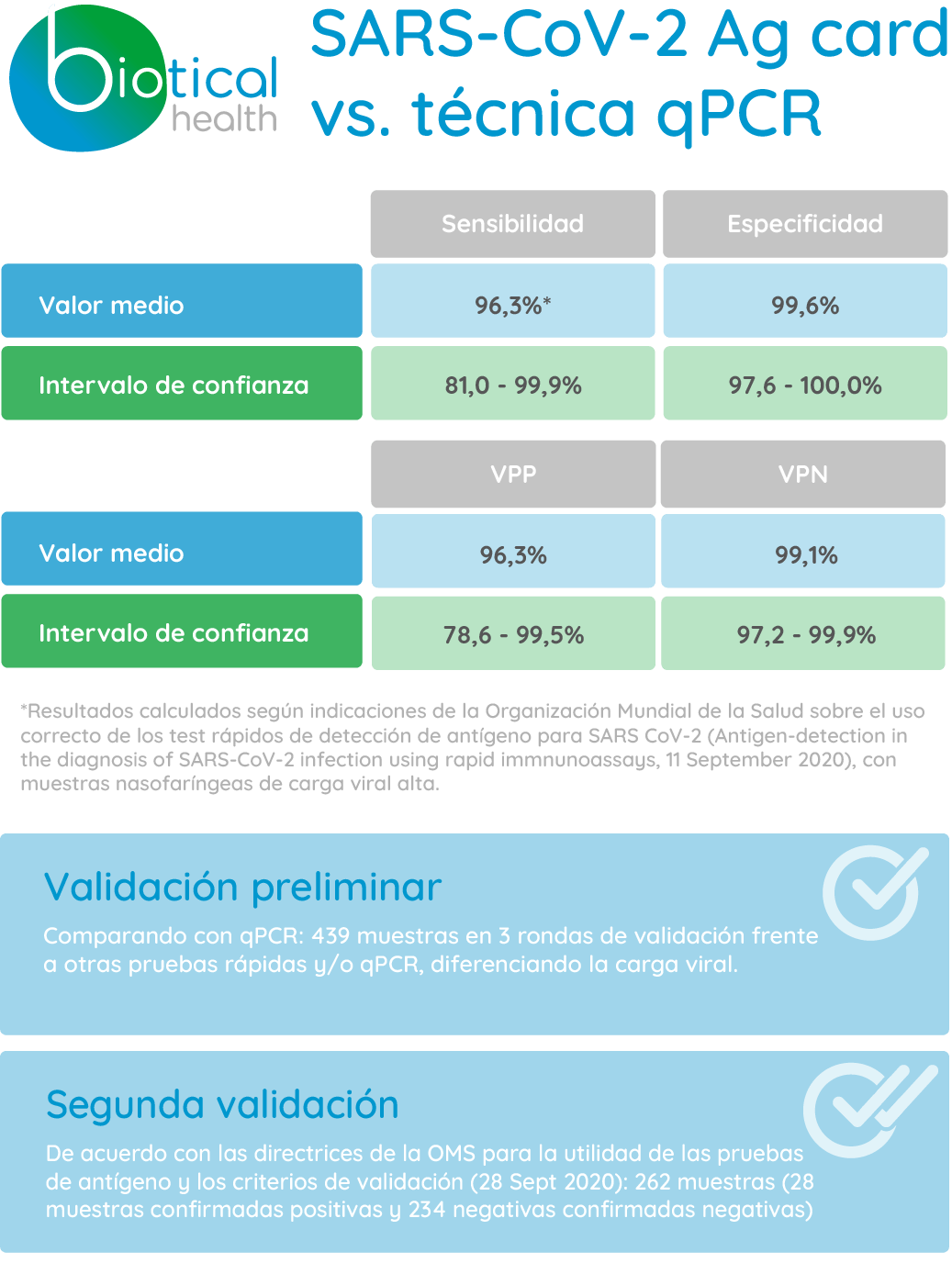
SARS-CoV-2 Ag card vs. técnica qPCR
| Sensibilidad | Especificidad | VPP | VPN | |
|---|---|---|---|---|
| Valor Medio | 96,3%* | 99,6% | 96,3% | 99,1% |
| Intervalo de confianza | 81,0 – 99,9% | 97,6 – 100,0% | 78,6 – 99,5% | 97,2 – 99,9% |
Validación preliminarComparando con qPCR: 439 muestras en 3 rondas de validación frente a otras pruebas rápidas y/o qPCR, diferenciando la carga viral. |
Segunda validaciónDe acuerdo con las directrices de la OMS para la utilidad de las pruebas de antígeno y los criterios de validación (28 Sept 2020): 262 muestras (28 muestras confirmadas positivas y 234 negativas confirmadas negativas) |


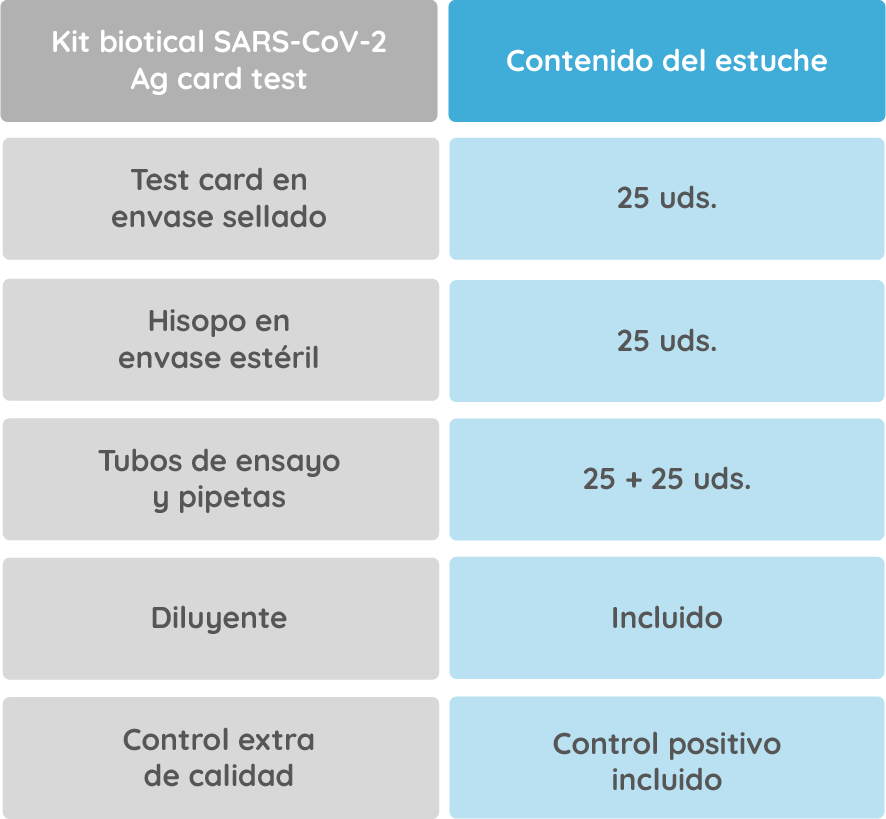
| Kit biotical SARS-CoV-2 Ag card test | Test card en envase sellado |
Hisopo en envase estéril | Tubos de ensayo y pipetas | Diluyente | Control extra de calidad |
|---|---|---|---|---|---|
| Contenido del estuche | 25 uds. | 25 uds. | 25 + 25 uds. | Incluido | Control Positivo incluido |

TELÉFONO
(+34) 91 677 43 08
WEB
DIRECCIÓN
Biotical Health, S.L.U.
C/ Sierra de Guadarrama, 1.
28830 San Fernando de Henares (Madrid) España
Importante
Este es un producto de catalogado como de “Diagnóstico In Vitro”, no es un producto de “Autodiagnóstico”, por tanto no puede ser vendido a personas particulares, sino a Hospitales, Centros de Salud, Clínicas, Laboratorios, Residencias de Ancianos, Servicios Públicos, Mutuas de Prevención de Riesgos o Empresas, siempre que se cumplan las directrices establecidas por la orden Ministerial publicada en el BOE de 14 de abril de 2020, en el que se establece que “se limita la realización de las pruebas diagnósticas para la detección del COVID-19 a aquellos casos en los que exista una prescripción previa por un facultativo y se ajusten a criterios establecidos por la autoridad sanitaria competente”





